Макрофаг
Главная функция макрофага – фагоцитоз. На его поверхности находится множество разных рецепторов, которые необходимы для захвата вирусов, грибов, бактерий, иммуноглобулинов. Фагоцитоз во время пролиферативного воспаления не всегда может быть завершенным, то есть не заканчивается абсолютным перевариванием чужеродного агента. Вирусы и микробные клетки внутри макрофагов выживают, размножаются, по причине чего процесс приобретает хроническую форму. Помимо макрофагов во время пролиферативного воспаления часто встречаются другие клетки. К ним следует отнести лимфоциты, эозинофилы, плазматические клетки, тучные клетки, единичные нейтрофилы.
При пролиферации клеток формируются клеточные диффузные либо очаговые инфильтраты.
Интерстициальное
Интерстициальное (или межуточное) – вид пролиферативного воспаления, при котором в строме сердца, печени, почек, легких формируется диффузный или очаговый клеточный воспалительный инфильтрат. Инфильтрат представляется лимфоцитами, плазматическими клетками, макрофагами, эозинофилами, тучными единичными клетками, элементами разрушенной паренхимы, редкими нейтрофилами.
В паренхиматозных элементах определяются выраженные дистрофические, в некоторых случаях некробиотические изменения. Итогом межуточного воспаления будет интерстициальный фиброз, представляющий собой разрастание соединительных тканей.
Как осуществляется пролиферация?
Пролиферация возникает в самом окончании воспалительного процесса, когда разрушение патологически влияющими на ткани бактериями и вирусами заканчивается. Признаки пролиферации можно заметить на той стадии, при которой разрушенные клетки начинают восстанавливаться, токсины — выводиться, а поврежденные ткани поверхности — восстанавливаться.
Конечно же, заметить простым взглядом, как сменяет пролиферация воспаление, невозможно. Все процессы проходят на внутриклеточном уровне. Вырабатывающийся на этой стадии белок б2-макроглобулин восстанавливает проницаемость сосудов, пониженную во время заболевания, защищает соединительную ткань от разрушений. Внутри клеток исчезают свободные радикалы, их нейтрализует супероксиддисмутаза – вещество, содержащееся в человеческом организме, антиоксидантный фермент. На этой стадии и происходит пролиферация. Что это клеточное возрождение, видно по процессам. Клетки перестают синтезировать патогенные медиаторы, и на их поверхности появляются новые рецепторы, здоровые. Старые же засасываются внутрь и уничтожаются.
С полипами и остроконечными кондиломами
Пролиферативная фаза воспаления с образованием полипов, а также остроконечных кондилом отличается хроническим течением. Она локализуется на слизистой оболочке. На слизистых разных органов формируются отдельные участки гиперплазии, а также разрастания эпителия в форме полипов, у которых соединительнотканная основа инфильтрирована макрофагами, лимфоцитами, плазматическими клетками и другими.
Локализуется чаще всего на слизистой оболочке носа, желудка, матки, кишечника, бронхов. В случае локализации воспалений на стыке однослойного цилиндрического и многослойного плоского эпителия формируются так называемые кондиломы. Эти образования частенько появляются в заднем проходе, а также на половых органах. При хроническом пролиферативном воспалении частая кондилома — это остроконечная, которая вызывается папилломавирусом. Она считается фактором риска для развития плоскоклеточной формы рака.
Пролиферация клеток и рак
Гормоны являются регуляторами роста клеток. Такие пептидные гормоны, как ГР, ИФР-1 и ИФР-2 стимулируют линейный рост тела и пролиферацию клеток многих тканей (гл. 7). Аналогичным действием обладают и другие пептиды [фактор роста фибробластов (ФРФ), тромбоци- тарный фактор роста (PDGF), ТФР-а и ТФР-JJ]. Тройные факторы регулируют рост эндокринных желез. Так, АКТГ и ангиотензин II влияют на размеры надпочечников, ТТГ — на размер щитовидной железы, а ЛГ и ФСГ — на размеры яичников и яичек. Тиреоидные гормоны стимулируют рост многих тканей. Стероидные гормоны могут как стимулировать, так и ингибировать рост клеток. Глюкокортикоиды ингибируют пролиферацию некоторых клеток и вызывают гибель лимфоцитов, тогда как эстрадиол, тестостерон и дигидротестостерон стимулируют рост соответственно молочных желез и предстательной железы.
Гормоны влияют на рост раковых клеток, причем часто таким же образом, что и на нормальные недиффенцированные клетки. Примером служит влияние эстрогенов на рак молочной железы и влияние андрогенов на рак предстательной железы. Однако причиной рака может быть и нарушение путей проведения гормональных сигналов. Как отмечалось выше, многие аналоги факторов роста и их рецепторы кодируются онкогенами.
Грануломатозное
Грануломатозное – еще один вариант продуктивного (пролиферативного) воспаления. Во время которого главным морфологическим субстратом считается гранулема, где преобладают клетки: макрофаги, а также их производные (гигантские клетки, эпителиоидные).
Морфогенез гранулем имеет из четыре последовательные фазы. К таковым относятся следующие:
- накопление молодых моноцитов в очаге повреждения;
- созревание данных клеток в макрофаге с формированием макрофагальной гранулемы;
- дальнейшее созревание и преобразование моноцитов и макрофагов в эпителиоидную клетку и формирование эпителиоидоклеточной гранулемы;
- трансформация эпителиоидной клетки в гигантскую клетку Пирогова-Лангханса (клетка инородных тел) и образование гигантоклеточных гранулем.
Следует отметить, что фагоцитарная активность клетки гранулемы по мере ее созревания постепенно снижается.
Диаметр гранулем составляет около 1-2 мм, чаще всего они видны лишь микроскопом. В центральной области гранулемы можно разглядеть тканевой детрит, который образуется в результате некроза тканей и в котором способен выявляться возбудитель основного заболевания, если в данном случае имеет место быть инфекционный процесс. Располагаются макрофаги по периферии некроза. Также там имеются гигантские, эпителиоидные клетки, среди них могут находиться еще плазматические клетки, нейтрофилы, лимфоциты, эозинофилы.
Грануломатозные болезни
Среди таких заболеваний при форме пролиферативного воспаления выделяют 4 группы. К ним относятся:
- инфекционной этиологии, куда следует отнести ревматизм, сыпной и брюшной тиф, бешенство, бруцеллез, туляремию, вирусный энцефалит, иерсинеоз, актиномикоз, сифилис, лепру, шистосомоз, туберкулез, склерому, сап и другие;
- неинфекционной этиологии, куда следует отнести подагру, силикоз, антракоз, талькоз, асбестоз, бериллиоз, алюминоз;
- медикаментозные недуги, например, лекарственный гепатит, олеогранулематозная болезнь;
- болезни не установленной этиологии: болезнь Крона, саркоидоз, болезнь Хортона, гранулематоз Вегенера, ревматоидный артрит, ксантогранулематозный пиелонефрит.
Абсолютно все гранулемы имеют инфекционную этиологию, не смотря на имеющиеся различия, по морфологии они сходны между собой. Также стоит отметить, что во всех ситуациях инфекционные гранулемы представляются в виде скоплений клеток, имеющих моноцитарно-макрофагальной природу. В некоторых гранулемах формируются лимфоциты, нейтрофилы, плазматические клетки, при гельминтозах появляется много эозинофилов.
Исключением будут лишь гранулемы в случае туберкулеза, сифилиса, склеромы, сапы, лепры. При названных болезнях при пролиферативном воспалении эти гранулемы обладают специфическими чертами, свойственными только определенному возбудителю. А это позволяет относить данную группу заболеваний к группе специфических гранулематозов. Или специфическое воспаление.
В морфологическом понятии для специфического воспаления будет характерно образование нескольких специфических гранулем. Которые имеют характерное строение. Оно может отличаться в зависимости от главного возбудителя — причины пролиферативного воспаления. Таким образом, клеточный состав, а также расположение клеток непосредственно в гранулеме довольно специфично для каждого возбудителя.
Главная / Издательство / Механизмы развития пролиферации в очаге воспаления
2.1.10. Механизмы развития пролиферации в очаге воспаления
Пролиферация является завершающей фазой развития воспаления, обес-печивающей репаративную регенерацию тканей на месте очага аль-
терации. Пролиферация развивается с самого начала воспаления наряду с яв-лениями альтерации и экссудации.
При репаративных процессах в очаге воспаления регенерация клеток и фиброплазия достигаются как активацией процессов пролиферации, так и ог-раничением апоптоза клеток. Размножение клеточных элементов начинается по периферии зоны воспаления, в то время как в центре очага могут еще про-грессировать явления альтерации и некроза. Полного развития пролиферация соединительнотканных и органоспецифических клеточных элементов дости-гает после «очистки» зоны повреждения от клеточного детрита и инфекци-онных возбудителей воспаления тканевыми макрофагами и нейтрофилами. В связи с этим следует отметить, что процессу пролиферации предшествует формирование нейтрофильного и моноцитарного барьеров, которые форми-руются по периферии зоны альтерации.
Восстановление и замещение поврежденных тканей начинается с выхода из сосудов молекул фибриногена и образования фибрина, который формиру-ет своеобразную сетку, каркас для последующего клеточного размножения. Уже по этому каркасу распределяются в очаге репарации быстро образую-щиеся фибробласты. Деление, рост и перемещение фибробластов возможны только после их связывания с фибрином или коллагеновыми волокнами. Эта связь обеспечивается особым белком – фибронектином. Размножение фиб-робластов начинается по периферии зоны воспаления, обеспечивая формиро-вание фибробластического барьера. Хемотаксис, активация и пролиферация фибробластов осуществляются под воздействием:
1. Факторов роста фибробластов.
2. Тромбоцитарного фактора роста.
3. Цитокинов — ФНО, ИЛ-1.
4. Кининов.
5. Тромбина.
6. Трансформирующего фактора роста b.
Сначала фибробласты не зрелые и не обладают достаточной синтетиче-ской активностью. Созреванию предшествует внутренняя структурно-функциональная перестройка фибробластов: гипертрофия ядра и ядрышка, гиперплазия ЭПС, повышение содержания ферментов, особенно щелочной фосфатазы, неспецифической эстеразы, b-глюкуронидазы. Только после пе-рестройки фибробласты начинают синтезировать коллаген, эластин, коллаге-нассоциированные белки и протеогликаны. Коллагеногенез стимулируется следующими биологически активными веществами — ФНО, ИЛ-1, ИЛ-4, фак-тором роста фибробластов, тромбоцитарным фактором роста.
Интенсивно размножающиеся фибробласты продуцируют кислые муко-полисахариды – основной компонент межклеточного вещества соединитель-ной ткани (гиалуроновую кислоту, хондроитинсерную кислоту, глюкозамин, галактозамин). При этом зона воспаления не только инкапсулируется, но и начинаются постепенная миграция клеточных и бесклеточных компонентов соединительной ткани от периферии к центру, формирование соединитель-нотканного остова на месте первичной и вторичной альтерации.
Наряду с фибробластами размножаются и другие тканевые и гематоген-ные клетки. При разрушении базальных мембран сосудов в зоне альтерации происходит миграция клеток эндотелия по градиенту ангиогенных факторов. Просвет новообразующегося капилляра формируется путем слияния внекле-точных пространств соседних эндотелиоцитов. Вокруг новообразующихся капилляров концентрируются тучные клетки, макрофаги, нейтрофилы, кото-рые освобождают биологически активные вещества, способствующие про-лиферации капилляров.
Важнейшими факторами, стимулирующими ангиогенез, являются:
1. Факторы роста фибробластов (основной и кислый).
2. Сосудистый эндотелиальный фактор роста.
3. Трансформирующие факторы роста .
4. Эпидермальный фактор роста.
Фибробласты вместе с вновь образованными сосудами создают грануля-ционную ткань. Это, по существу, молодая соединительная ткань, богатая клетками и тонкостенными капиллярами, петли которых выступают над по-верхностью ткани в виде гранул.
Основными функциями грануляционной ткани являются: защитная – пре-дотвращение влияния факторов окружающей среды на очаг воспаления и ре-паративная – заполнение дефекта и восстановление анатомической и функ-циональной полноценности поврежденных тканей.
Формирование грануляционной ткани не строго обязательно. Это зависит от величины и глубины повреждения. Грануляционная ткань обычно не раз-вивается при заживлении ушибленных кожных ранок или мелких поврежде-ний слизистой оболочки (Кузин М.И., Костюченок Б.М. и соавт., 1990). Гра-нуляционная ткань постепенно превращается в волокнистую ткань, называе-мую рубцом. В рубцовой ткани уменьшается количество сосудов, они запус-тевают, уменьшается количество макрофагов, тучных клеток, снижается ак-тивность фибробластов. Небольшая часть клеточных элементов, распола-гающаяся среди коллагеновых нитей, сохраняет активность. Предполагают, что сохранившие активность тканевые макрофаги принимают участие в рас-сасывании рубцовой ткани и обеспечивают формирование более мягких руб-цов.
Параллельно с созреванием грануляций происходит эпителизация раны. Она начинается в первые часы после повреждения, и уже в течение первых суток образуются 2-4 слоя клеток базального эпителия. Скорость эпителиза-ции обеспечивается следующими процессами: миграцией, делением и диф-ференцировкой клеток. Эпителизация небольших ран осуществляется, в ос-новном, за счет миграции клеток из базального слоя. Раны более крупные эпителизируются за счет миграции и митотического деления клеток базаль-ного слоя, а также дифференцировки регенерирующего эпидермиса. Новый эпителий образует границу между поврежденным и подлежащим слоем, он препятствует обезвоживанию тканей раны, уменьшению в ней электролитов и белков, а также предупреждает инвазию микроорганизмов.
В процессе пролиферации участвуют и органспецифические клеточные элементы органов и тканей. С точки зрения возможностей пролиферации ор-ганспецифических клеточных элементов все органы и ткани могут быть рас-классифицированы на три группы:
К первой группе могут быть отнесены органы и ткани, клеточные элемен-ты которых обладают активной или практически неограниченной пролифе-рацией, достаточной для полного восполнения дефекта структуры в зоне воспаления (эпителий кожи, слизистых оболочек дыхательных путей, слизи-стой желудочно-кишечного тракта, мочеполовой системы; гемопоэтическая ткань и др.).
Ко второй группе относятся ткани с ограниченными регенерационными способностями (сухожилия, хрящи, связки, костная ткань, периферические нервные волокна).
К третьей группе относятся те органы и ткани, где органоспецифические клеточные элементы не способны к пролиферации (сердечная мышца, клетки ЦНС). Основными факторами, регулирующими процессы пролиферации и дифференцировки клеток в очаге воспаления, являются:
1. Факторы роста, продуцируемые макрофагами, лимфоцитами, тромбо-цитами, фибробластами и другими клетками, стимулированными в зоне вос-паления. К ним относятся:
— факторы роста эпидермиса (стимулятор пролиферации и созрева-ния эпителия, стимулятор ангиогенеза);
— трансформирующий фактор роста- (стимулятор ангиогенеза);
— трансформирующий фактор роста- (хемоаттрактант фибробла-стов, стимулятор синтеза коллагена, фибронектина, ангиогенеза, ингибитор протеолиза);
— тромбоцитарный фактор роста (стимулятор миграции, пролифе-рации и синтеза белка в клетках-мишенях, обладает провоспалительным эф-фектом);
— фактор роста эндотелиоцитов;
— фактор роста фибробластов кислый и основной (стимуляторы пролиферации всех клеток сосудистой стенки);
— колониестимулирующие факторы (гранулоцитарный и макрофа-гальный стимуляторы дифференцировки, пролиферации и функциональной активности клеток гранулоцитарного и моноцитарного ряда) — цитокины (ФНО, ИЛ-1, ИЛ-2, ИЛ-3, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-7) , продуцируемые Т- и В-лимфоцитами, мононуклеарами, тучными клетками, фибробластами, эндоте-лиоцитами, обеспечивают хемотаксис, фиброгенез, ингибируют апоптоз, стимулируют процессы пролиферации в очаге воспаления. Ингибиторами роста для некоторых клеток служат те же цитокины, которые стимулируют пролиферацию других – это ФНО, трансформирующий фактор роста и - интерферон (Зайчик А.Ш., Чурилов Л.П., 1999);
— фактор роста нервов (стимулятор пролиферации, роста, морфоге-неза симпатических нейронов, эпителиальных клеток). Ростовые факторы, взаимодействуя с рецепторами на клетках- мишенях, могут непосредственно стимулировать синтез ДНК в клетках или подготавливать внутриклеточные рецепторы и ферменты к митотической деятельности.
2. Пептид гена, родственного кальцитонину, стимулирует пролифе-рацию эндотелиальных клеток, а субстанция Р индуцирует выработку ФНО в мак-рофагах.
3. Простагландины группы Е потенцируют регенерацию путем усиления кровоснабжения.
4. Кейлоны и антикейлоны, продуцируемые различными клетками, дейст-вуя по принципу обратной связи, могут активировать и угнетать митотиче-ские процессы в очаге воспаления (Бала Ю.М., Лифшиц В.М., Сидельникова В.И., 1988).
5. Полиамины (путресцин, спермидин, спермин), обнаруживаемые во всех клетках млекопитающих, жизненно необходимы для роста и деления клеток.
Они обеспечивают стабилизацию плазматических мембран и суперспи-ральной структуры ДНК, защиту ДНК от действия нуклеаз, стимуляцию транскрипции, метилирование РНК и связывание ее с рибосомами, актива-цию ДНК-лигаз, эндонуклеаз, протеинкиназ и многие другие клеточные про-цессы. Усиленный синтез полиаминов, способствующих пролиферативным процессам, отмечается в очаге альтерации (Березов Т.Т., Федорончук Т.В., 1997).
6. Циклические нуклеотиды: цАМФ ингибирует, а цГМФ активирует про-цессы пролиферации.
Заживление раны.
Морфологически процесс заживления раны может протекать различно, в зависимости от анатомического субстрата поражения, степени инфицирован-ности, общего состояния организма, характера лечебных мероприятий (Ку-зин М.И., Костюченок Б.М. и соавт., 1990). Однако в любом случае течение раневого процесса отражает один из классических типов заживления:
1. Заживление первичным натяжением.
2. Заживление вторичным натяжением.
3. Заживление под струпом.
Заживление раны первичным натяжением. Такой тип заживления харак-теризуется сращением краев раны без видимой промежуточной ткани, путем соединительнотканной организации раневого канала. Заживление первичным натяжением является наиболее экономичным видом заживления. Для зажив-ления первичным натяжением необходимы следующие условия:
1. Небольшая зона повреждения.
2. Плотное соприкосновение краев раны.
3. Сохранение жизнеспособности краев раны.
4. Отсутствие очагов некроза и гематомы.
5. Асептичность раны.
Морфологическая картина заживления первичным натяжением проявля-ется умеренной гиперемией, отеком тканей в стенках раны, пролиферацией фибробластов и новообразованием капилляров путем эндотелизации каналов и щелей в сгущающемся фибрине (аутохтонный механизм) от одного края раны к противоположному. На 6-8-й день грануляционная ткань прочно со-единяет стенки раны, и в этот период прекращается эпителизация. В хирур-гической практике заживление первичным натяжением возможно в двух слу-чаях: при небольших размерах раны (края отстают не более 10 мм друг от друга), а также при хирургических вмешательствах, заканчивающихся нало-жением швов. Местные изменения в области раны выражены незначительно (отечность краев, гиперемия, инфильтрация, боль). К общим проявлениям относится повышение температуры тела, которая постепенно снижается к 3-м суткам после операции. Изменения морфологического состава крови вы-ражены незначительно или отсутствуют. Иногда отмечаются нейтрофильный лейкоцитоз и увеличение СОЭ до 20 мм/ч. На 5-6-е сутки эти показатели обычно нормализуются.
Заживление раны вторичным натяжением происходит при обширных по-вреждениях тканей, при наличии в ране нежизнеспособных тканей, гематомы и при развитии инфекции в ране. Любой из этих факторов ведет к заживле-нию вторичным натяжением. При различных вариантах течения заживления вторичным натяжением речь идет о заживлении гнойной раны, то есть о за-живлении через нагноение и гранулирование. На 5-6-е сутки после альтера-ции, после отторжения некротизированных клеток в ране появляются ост-ровки грануляций, которые, постепенно разрастаясь, заполняют всю полость раны. Изменения характера грануляций всегда объективно отражают ослож-нения заживления, которые могут наступить под влиянием местных и общих факторов. Реорганизация рубца проявляется активной эпителиизацией раны. Эпителий нарастает на поверхность грануляций в виде голубовато-белой каймы очень медленно. Помимо эпителизации заживлению способствует фе-номен раневой контракции — равномерного концентрического сокращения краев и стенок раны. Этот феномен объясняется появлением в грануляцион-ной ткани в период регенерации фибробластов, обладающих способностью к сокращению.
Заживление раны под струпом характерно для незначительных повреж-дений (ссадины, царапины, небольшие по площади ожоги 1-й и 2-й степени). Раневой процесс начинается свертыванием излившейся крови или только лимфы, которая подсыхает с образованием струпа. Под ним происходит бы-страя регенерация эпидермиса, и струп затем отторгается. Весь процесс длится 3-7 дней. Если заживление под струпом происходит без осложнений, то рана заживает первичным натяжением; если под струпом начинается на-гноение, то заживление идет по типу вторичного натяжения. В ряде случаев может развиться вялотекущее флегмонозное поражение жировой клетчатки, окружающей рану. В такой ситуации необходимы хирургическая обработка раны и удаление струпа (Кузин М.И., Костюченок Б.М. и соавт., 1990).
предыдущий раздел | содержание| следующий раздел
При туберкулезе
Воспалительный процесс при туберкулезе, то есть микобактерия туберкулеза способна вызывать три разновидности тканевой реакции: экссудативную, альтеративную, и пролиферативную.
Что касается альтеративного воспаления, то оно чаще развивается в результате гипоергии, в случае снижения защитных сил человеческого организма. Проявляется данное воспаление морфологически казеозным некрозом.
Экссудативный тип воспаления развивается в результате имеющейся гиперергии (в случае повышенной чувствительности к токсинам микобактерии, антигенам). Морфологически накопление проявляется в очаге поражения фибринозного, серозного либо смешанного экссудата, в дальнейшем который подвергается тоже казеозному некрозу.
Пролиферативное воспаление, патанатомия говорит, развивается в условии специфической туберкулезной иммунной системы. Морфологическим проявлением в данном случае будет выступать образование так называемых туберкулезных гранулем, представленных в виде просяного зерна.
Водно-солевой обмен
Гормоны регулируют многие стороны водно-солевого обмена. Так, вазопрессин изменяет осмо- ляльность сыворотки и экскрецию воды (гл. 6) и влияет на многие функции сердечно-сосудистой системы и ЦНС. Минералокортикоид альдостерон регулирует соотношение ионов натрия и калия, а также, в некоторой степени, соотношение ионов хлорида и бикарбоната. В регуляции ионного баланса принимают участие и другие гормоны — ПНП, инсулин, глюкагон, катехоламины, ангиотензин II и ПТГ.
Следующие:
- Успехи современной науки и эндокринология. 1 часть
- Костная ткань. Репродуктивная система. Иммунная система. Центральная нервная система
- Промежуточный обмен. Водно-солевой обмен. Сердечно-сосудистая система и почки
Туберкулезная гранулема
Итак, мы разобрали, чем характеризуется пролиферативное воспаление. Теперь стоит по отдельности рассмотреть некоторые случае, при которых оно проявляет себя.
Туберкулезная гранулема обладает характерным строением: в центральной ее области находится очаг так называемого казеозного некроза, за которым располагается вал радиарно локализующихся (то есть вытянутых по-длиннику к периферии от центра) эпителиоидных клеток. За этими клетками видны гигантские единичные клетки Пирогова-Лангханса.
Следует также заметить, что на периферии такой гранулемы находится вал лимфоцитов. В большом количестве данных типичных клеток обнаружены могут быть еще в незначительном количестве плазматические клетки, а также макрофаги. Кроем того, здесь же выявляется тоненькая сеть, состоящая из аргирофильных волокон. Что касается кровеносных сосудов, то они тут не встречаются. В случае окраски по Цилю-Нильсену в данных гигантских клетках могут быть определены микобактерии туберкулеза.
Промежуточный обмен
Инсулин, глюкагон, соматостатин, ГР, катехоламины (адреналин, норадреналин), тиреоидные гормоны, глюкокортикоиды и другие гормоны регулируют обмен углеводов, жиров, белков, аминокислот и нуклеиновых кислот. В регуляции промежуточного обмена гормоны действуют координировано, осуществляя приспособление организма к разнообразным условиям существования, таким, как стресс или голодание. Инсулин снижает уровень глюкозы в крови и стимулирует синтез жира, белков и нуклеиновых кислот, тогда как кортизол, глюкагон, катехоламины и ГР, напротив, действуя различными способами, повышают уровень глюкозы в крови. На обмен белков, жиров и нуклеиновых кислот эти гормоны влияют по-разному. Гормоны изменяют поглощение глюкозы, аминокислот, нуклеозидов и других малых молекул клетками. Например, инсулин усиливает поглощение глюкозы, вызывая перемещение ее транспортеров к плазматической мембране. Гормоны влияют также на количество и активность ферментов, участвующих в промежуточном обмене — глюконеогенезе, липолизе, синтезе гликогена, метаболизме и синтезе аминокислот, синтезе липидов и т.д.
Воспалительный процесс при сифилисе
Воспалительный процесс при сифилисе в разные периоды будет отражать на бледную трепонему различную тканевую реакцию: выделяют, как правило, первичный, вторичный, а также третичный периоды при заболевании сифилисом.
В случае первичного сифилиса развивается так называемая продуктивно-инфильтративная реакция в области внедрения трепонемы.
Во время вторичного наблюдается сильно выраженная экссудативная реакция, способствующая генерализации возбудителя,
В случае третичного периода сифилиса продуктивно-некротическая реакция будет представлена в виде сифилитической гранулемы, а также гуммозными инфильтратами.
Подробнее о сифилитической гранулеме
Сифилитическая гранулема в области медицины также носит короткое название «гумма». В данной гранулеме, как и в случае с туберкулезом, в центре обнаруживается казеозный некроз, однако в этой ситуации он будет более крупный по размеру.
От некроза по периферии располагается большое количество лимфоцитов, фибробластов, а также плазматических клеток. В небольшом количестве здесь могут присутствовать и макрофаги, и гигантские клетки, и эпителиоидные клетки. Характерным считается в данном случае разрастание соединительных тканей (это связано с быстротой пролиферации фибробластов), которые формируют подобие капсул, а также большое количество кровеносных сосудов.
Довольно редко среди этих клеток удается специалистам выявить так называемую бледную трепонему методом серебрения по Левадити. Характерна гумма для третичного периода сифилиса, который начинает развиваться через несколько лет (5 и больше) со времени его заражения.
В различных органах: коже, печени, костях, головном мозге образуются в течение одного десятка лет узлы размером 0,3-1,0 см в диаметре. В разрезе из данных узлов выделяется некая желеобразная масса желтоватого оттенка, которая по своему внешнему виду напоминает клей гуммиарабик, откуда и произошло такое название «гумма».
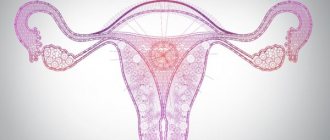
Пролиферация в гинекологии
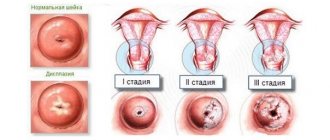
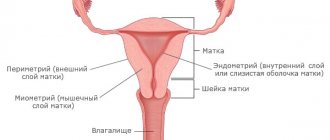
В жизненном цикле женщины детородного возраста пролиферация происходит регулярно. Во время менструации эндометрий отторгается, затем восстанавливается. Поэтому при взятии гистероскопии – соскоба со стенки матки — или при исследовании на аппарате УЗИ очень важно учитывать, какая фаза пролиферации эндометрия. В течение месячного цикла эндометрий имеет различную толщину, и именно по нему и судят о работе детородных органов женщины.
Фаза роста эндометрия — очень важный параметр для оценки патоморфологической картины. Без знания этого параметра точный диагноз поставить невозможно даже опытному специалисту.
Гуммозная инфильтрация
Кроме этих гумм, в третичном периоде заболевания сифилисом может развиваться также гуммозная инфильтрация. Представлен инфильтрат теми же клетками, то есть склерозом, сосудистой пролиферацией. Инфильтрат локализуется чаще всего в восходящем отделе сердца, а также дуге аорты, а носит название «сифилитический мезоаортит».
Он, расположенный в центральной и наружной оболочке сердечной аорты разрушает постепенно эластический ее каркас, а на месте эластических волокон начинает разрастаться соединительная ткань. По причине всего этого внутренняя оболочка на аорте становится неровной и морщинистой с большим количеством рубцовых втяжений, выбуханий, внешне напоминая шагреневый кожный покров.