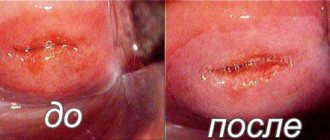
Рак шейки матки (РШМ) на протяжении последних лет занимает лидирующие позиции среди проблем онкологии и гинекологии, сохраняются высокие показатели заболеваемости и смертности, несмотря на повышенный интерес к проблеме и многочисленные исследования в данной области [1—3]. Отсутствие в нашей стране первичной массовой профилактики РШМ путем вакцинации, рост инфицированности высокоонкогенными штаммами вируса папилломы человека (ВПЧ) среди населения земного шара [4—7], высокая частота фоновых заболеваний шейки матки, способствующих процессу карциногенеза [8—10], обусловливают особую значимость разработки методов вторичной профилактики. Основными направлениями в данной области являются изучение факторов риска опухолевой трансформации с целью их своевременной коррекции, совершенствование методов скрининга и разработка новых алгоритмов ведения, направленных на повышение эффективности терапии и профилактику рецидивов дисплазии шейки матки [11—14]. Особое место занимает решение вопроса реабилитации нарушений репродуктивного здоровья пациенток, пролеченных по поводу дисплазии, учитывая основной прирост заболеваемости РШМ среди пациенток активного репродуктивного возраста [15—17].
Пусковым механизмом карциногенеза является длительное персистирование папилломавирусов в клетках эндо- и экзоцервикса с развитием иммунной несостоятельности и структурных изменений на клеточном и тканевом уровнях, приводящих к возникновению преинвазивной патологии [5, 18, 19]. Однако сам факт инфицирования не является единственной причиной, необходимой для возникновения опухоли [20—22]. У большинства инфицированных женщин, особенно в молодом возрасте, при правильной тактике ведения можно добиться элиминации возбудителя до начала развития диспластического процесса [14, 23, 24]. Своевременная диагностика и адекватное лечение фоновой патологии шейки матки, определение и коррекция факторов риска позволяют предотвратить развитие дисплазии шейки матки и последующий карциногенез. Комплексная лечебная тактика с применением современных высокоэффективных органосберегающих методик терапии обеспечивает возможность излечения почти у 98% пациенток с преинвазивными процессами и карциномой in situ
[8, 15, 25]. Однако сформировавшиеся тенденции в лечении больных с CIN в основном направлены на удаление патологического очага, что приводит к избыточной, в ряде случаев необоснованной хирургической агрессии c развитием осложнений, в том числе в виде анатомической несостоятельности шейки матки, невынашивания беременности и осложненного течения родов [24, 26]. Общепринятые методики терапии часто не предусматривают стимуляции системного противовирусного эффекта и проведения этапа реабилитации после эксцизионного вмешательства, что может обусловливать рецидив заболевания [14, 27, 28].
Согласно данным литературы [16, 20, 29], к предрасполагающим факторам рецидива CIN II—III после хирургического органосохраняющего лечения относятся: повторное заражение ВПЧ в раннем послеоперационном периоде или наличие положительного теста с полимеразной цепной реакцией (ПЦР-теста) после выполнения эксцизии (вирус-позитивный край резекции), нарушение процессов метилирования в прилежащих тканях, особенно в сочетании с активным или пассивным курением, а также наличие в крае резекции конуса диспластических клеток вне зависимости от степени их изменений.
Из полученных данных следует, что удаление патологического очага необходимо, но недостаточно для купирования карциногенеза и предотвращения рецидива.
Цель исследования — усовершенствование алгоритма ведения пациенток с рецидивирующей тяжелой дисплазией цервикального эпителия.
Конизация при дисплазии шейки матки
Конизацией шейки матки называется операция, которая предполагает конусообразное иссечение слизистого эпителия цервикального канала. Свое название процедура получила от формы удаляемого сегмента.
Конизация шейки матки при дисплазии 3 степени является одним из эффективных вариантов лечения патологии. Заболевание считается достаточно опасным, так как имеет высокий риск малигнизации. При дисплазии шейки матки происходит разрастание атипичных клеток в зоне совмещения плоского эпителия с цилиндрическим.
Конизация при дисплазии шейки матки преследует основную цель: удаление атипичных клеток с цервикального канала и остановку патологического процесса. Процедура позволяет не только прекратить деление клеток, но и определяет начальные стадии рака.
Диагностика удаленного участка осуществляется для всех женщин, прошедших конизацию. Ткани подвергаются гистологическому исследованию, по результатам которого можно подтвердить или опровергнуть инвазивный рак.
Выявление опасного заболевания на ранних стадиях позволяет получить эффективное и своевременное лечение. Оперативное вмешательство осуществляется не только при дисплазии 3 степени. Показаниями для его проведения будут различные нарушения в эпителиальном слое: эрозия, рубцевание, деформация, эктропион шейки, а также дисплазия 2 и 4 степени.
В чем отличие эрозии и дисплазии шейки матки
Эрозия – это хроническое воспаление шейки матки. В современной гинекологии различают истинную эрозию и псевдоэрозию. Истинная проявляется довольно редко. Предпосылки для ее развития создаются на фоне серьезных травм шейки в ходе оперативных вмешательств. На поверхности образуется кровоточащая рана. Псевдоэрозия шейки матки или эктопия диагностируется при выявлении нетипичных клеток, внутреннего слоя, выстилающего матку наружу.
Дисплазия шейки матки гораздо опаснее. Такое состояние относят к классу предраковых. На фоне течения процесса проявляются изменения в строении клеток слизистой оболочки, выстилающей матку. Происходит утолщение, разрастание тканей и нарушается их функциональное предназначение.
Рассматривая отличие двух гинекологических состояний, стоит отметить, что эрозия захватывает только поверхностные эпителиальные слои в отличие от дисплазии. При дисплазии патологический процесс распространяется на все 3 слоя. Главная опасность обеих заболеваний проявляется при их несвоевременном обнаружении, потому женщинам в возрасте от 25 до 35 лет обязательно нужно проходить осмотр у гинеколога 1 раз в год. Необходимо не только визуальное обследование, но и расширенная кольпоскопия, потому что обнаружить атипичные клетки невооруженным взглядом – невозможно.
Симптоматики патологических состояний представлена в таблице.
| Клиническая картина характерная для эрозии и дисплазии шейки матки | |
| Эрозия | Дисплазия |
| Часто протекает в скрытой форме, потому диагностика осложнена. Кровянистые выделения могут проявляться после полового акта, спринцеваний или гинекологического осмотра. При присоединении бактериальной инфекции возникает зуд и жжение половых органов, появляются обильные выделения из влагалища с неприятным запахом. |
Внимание! Не следует пытаться определить диагноз и назначить лечение самостоятельно. Промедление в случае с дисплазией – опасно. В условиях отсутствия лечения легкая дисплазия перетекает в тяжелую, а затем в плоскоклеточный рак.
Эрозия, как и дисплазия, является самостоятельной нозологической единицей. Между этими заболеваниями есть только одна связь: опасное предраковое состояние развивается на последней стадии эрозии. В этом случае есть риск стремительного образования злокачественной опухоли.
Противопоказания
Если у женщины обнаружена дисплазия шейки матки, конизация осуществляется не всегда. Данный вид лечения противопоказан пациенткам с подтвержденным раком. В таком случае обычно удаляется орган целиком, после чего назначается длительное лечение, включающее в себя химиотерапию и облучение.
Запрещено делать конизацию, если у женщины имеется воспалительный процесс во влагалище. Необходимо сначала пройти лечение, а потом проводить выбранную методику оперативного вмешательства. Противопоказана конизация пациенткам во время беременности, так как это может стать причиной ее прерывания. Перед тем, как сделать конизацию, требуется подготовка и обследование.
Процедура прижигания дисплазии у нерожавших девушек
Для лечения дисплазии у нерожавших женщин редко используется метод электрокоагуляции. Связано это с тем, что после процедуры на поверхности шейки матки женщины образуется заметный, грубый рубец, который может препятствовать зачатию и усложнять процесс вынашивания беременности. Медики всегда пытаются сохранить детородную функцию женщины, потому отказываются от такой процедуры, чтобы не провоцировать бесплодие.
Чаще всего используется радиоволновой метод и лазерное прижигание. Такие терапевтические манипуляции позволяют вылечить дисплазию у нерожавших девушек без нарушений репродуктивной функции.
Подготовка
Дисплазия шейки матки зачастую имеет бессимптомное течение. Заболевание формируется в течение длительного времени, переходя из одной стадии в другую. Определить наличие несвойственных для отдельного участка шейки клеток можно во время гинекологического осмотра. Однако с уверенностью поставить диагноз нельзя. Чтобы убедиться в дисплазии, проводят кольпоскопию.
Кольпоскопия – детальное изучение слизистого слоя шейки матки с использованием увеличительного прибора и реагентов. Диагностика позволяет осмотреть патологические участки и взять ткани для дальнейшего изучения – сделать биопсию. Кольпоскопия является обязательным обследованием перед проведением конизации.
Если результаты кольпоскопии показывают, что шейка матки не имеет злокачественных новообразований, то осуществляется дальнейшая подготовка к операции:
- мазок из влагалища – определяет степень чистоты и помогает убедиться в отсутствии инфекционных процессов;
- анализы крови – в перечень основных входит общее исследование, биохимия, ТОРЧ-инфекции, а также определение группы и резуса;
- коагулограмма – устанавливает скорость сворачивания крови, что важно для предотвращения кровотечений;
- анализ мочи – позволяет оценить функциональность мочеобразующей системы, а также дает косвенную оценку работе организма;
- ПЦР-диагностика – необходима для определения ВПЧ в организме, который зачастую становится провокатором заболевания.
Чтобы восстановительный период прошел максимально гладко и легко, конизацию необходимо делать в первые дни менструального цикла, сразу после завершения кровотечения. Лечение обычно назначается на 5-7 день, но может быть проведено и на 10. Необходимость выполнения процедуры в первой фазе цикла обусловлена гормональным фоном пациентки.
Сразу после завершения ежемесячного кровотечения начинается выработка эстрогенов. Эти гормоны помогают слизистой оболочки восстановиться. Поэтому при проведении конизации в первой фазе риск осложнений минимизируется.
Дисплазия 3 степени может быть обнаружена у пациенток, находящихся в менопаузе. Если у женщины нет менструального цикла, то операция проводится в любой день.
Результаты и обсуждение
Анализ факторов риска рецидивирования диспластических процессов в шейке матки у больных показал, что не использовали контрацепцию 17 (27,4%) пациенток 1-й основной и 16 (26,7%) — 1-й контрольной групп. Частота применения различных методов контрацепции в основной и контрольной группах не различалась.
Деструктивные методы лечения в анамнезе до верификации диагноза CIN отмечены одинаково часто у женщин с рецидивом СIN и в контрольной группе: у 56 (90,3%) и 53 (88,3%) пациенток соответственно, в том числе неоднократные — у 35 (56,5%) и 25 (41,7%) пациенток основной и контрольной групп (p
>0,05). В структуре методов деструкции у больных обеих групп преобладала диатермокоагуляция (48,3 и 45%); реже — криолечение (29 и 25%) и радиоволновая терапия (РВТ) (23,2 и 20%).
Анатомические изменения на шейке матки отмечены у 27 (43,5%) женщин с рецидивом CIN. У 14 (22,6%) пациенток отмечены рубцовая деформация и гипертрофия шейки матки, у 7 (11,3%) — истмико-цервикальная недостаточность (ИЦН), у 6 (9,7%) выраженная гипертрофия органа была обусловлена множественными ретенционными кистами. Смещение зоны трансформации в цервикальный канал, затрудняющее проведение кольпоскопического и цитологического исследований, отмечено у большинства пациенток, перенесших деструктивные воздействия на шейку матки (42 женщины, или 68%). В контрольной группе анатомические изменения шейки матки диагностировались несколько реже — у 30 (50%) женщин (р
>0,05).
Диагноз CIN II—III вв. 1-й основной группе первоначально установлен на основании точечной прицельной биопсии у 46 (74,5%) пациенток, эксцизионное диагностическое вмешательство произведено — у 16 (25,8%). Выскабливание цервикального канала на этапе обследования выполнено у 23 (37,1%) женщин. При последующем выполнении лечебной эксцизии дополнительные очаги тяжелой дисплазии в удаленном конусе выявлены у 14 (22,6%) обследованных, недиагностированная CIN в цервикальном канале — у 3 (4,8%), что подтверждает данные [10] о гиподиагностике тяжелых поражений цервикального эпителия при проведении точечных биопсий.
Сочетанная патология влагалища и вульвы отмечена у 52 (83,8%) пациенток основной группы. В контрольной группе аналогичный показатель был достоверно ниже и составил 32 (53,3%) наблюдения (р
≤0,05). В структуре вульвовагинальной патологии при рецидивировании дисплазии преобладал бактериальный вагиноз у 37 (59,6%) пациенток, хронический вагинит диагностирован у 15 (24,2%), аногенитальные кондиломы — у 18 (29%). Пролапс стенок влагалища, сопровождающийся повышением рН более 4,5, (53,3%;
р
≤0,001), отмечен у 16 (25,8%) женщин основной группы, что достоверно чаще, чем в контрольной — 6 (10%) (
р
≤0,05).
Курящие пациентки составили большинство основной группы — 43 (69,4%), в контрольной группе их было значительно меньше — 21 (35%) (р
≤0,001).
Избыточная масса тела и пролапс стенок влагалища в основной группе отмечались достоверно чаще, чем в контрольной, составив соответственно 37,1% против 20% (р
≤0,05) и 25,8% против 10% (
р
≤0,05). Более 3 половых партнеров имели 37 (59,7%) пациенток основной и 12 (20%) наблюдаемых контрольной группы (
р
≤0,001).
Локализация дисплазии на экзоцервиксе отмечалась у большинства пациенток в контрольной группе — 50 (83,3%), в то время как в группе с рецидивом CIN достоверно чаще наблюдаются эндоцервикальная локализация и сочетание эндо- и экзоцервикального расположения CIN — 24 (38,8%) против 10 (16,6%) в контрольной группе (р
≤0,01).
Сочетанная гинекологическая патология отмечена у 41 (66,1%) женщины основной группы и у 35 (58,3%) — в контрольной (р
>0,05). В структуре патологии преобладали хронические воспалительные процессы в органах малого таза (51,6%) и гиперпластические процессы в репродуктивных органах: миома матки (25,8%), гиперпластические процессы в эндометрии (17,1%), эндометриоз (19,5%). Нарушения менструальной функции отмечены у 31,7% женщин 1-й основной группы. Следует отметить, что у 3 (4,8%) обследованных пациенток с рецидивом CIN III диагностирована сочетанная атипическая гиперплазия эндометрия. Сочетанная патология молочных желез диагностирована у 29 (46,7%) пациенток 1-й основной группы. В структуре патологии очаговые образования (кисты, фибромы) составили 17,7 и 24,1% соответственно, диффузные (фиброзная и фиброзно-кистозная мастопатии) — 28,4%. Различий в структуре патологии органов репродуктивной системы в основной и контрольной группах не выявлено.
Клинические и лабораторные признаки гиперандрогении выявлены у 13 (20,9%) пациенток основной и у 9 (15%) контрольной группы.
Среди женщин основной группы при первичном лечении только хирургическая деструкция патологического очага (ножевая, радиоволновая хирургия, диатермокоагуляция) была использована у 30 (48,4%), сочетание деструкции со стимуляцией противовирусного иммунитета — у 32 (51,6%), дополнительные методики лечения на этапе реабилитации — у 16 (25,8%) пациенток, фотодинамическая терапия — у 1 (1,6%), гормональное лечение по поводу сопутствующей патологии назначалось 12 (19,3%) женщинам. В контрольной группе стимуляция противовирусного иммунитета после эксцизии проводилась чаще: у 42 (70%) женщин (р
<0,05), в том числе фотодинамическая терапия — у 26 (43,3%) (
р
<0,001), таргетные* препараты назначались 28 (46,7%) (
р
<0,05), коррекция по поводу выявленных сочетанных гормональных нарушений (полипы, нарушения менструальной функции, гиперандрогения) — у 16 (26,7%;
р
>0,05) женщин.
Сочетанная патология влагалища и вульвы чаще диагностировалась в основной по сравнению с контрольной группой — 52 (83,8%) и 32 (53,3%) соответственно (р
≤0,01).
Положительный ПЦР-тест через 8 нед после проведения эксцизии отмечен у 20 (32,3%) пациенток основной и лишь у 5 (8,3%) контрольной группы (р
≤0,001). Обследование и лечение полового партнера у 49 (70,9%) пациенток основной группы не проводилось.
Таким образом, факторами риска рецидивирования CIN II—III являются: наличие большого числа половых партнеров и отсутствие их лечения, курение, нарушение влагалищного микробиоценоза, неоднократные деструктивные воздействия по поводу фоновых заболеваний шейки матки, приводящие к деформации органа, эндоцервикальная локализация диспластического процесса, наличие сопутствующей патологии органов репродуктивной системы, повторные хирургические вмешательства, обусловленные неадекватным диагностическим объемом первичной биопсии, ограничение лечения деструкцией патологического очага, наличие ВПЧ-позитивного края резекции после эксцизии.
Полученные результаты подтверждают данные литературы о влиянии курения, большого числа половых партнеров и ощелачивания влагалищной среды на процессы карциногенеза [1, 7, 25, 28], а также о сходных процессах патогенеза гиперпластических и диспластических процессов в органах репродуктивной системы [2].
Время наступления рецидива колебалось от 6 мес до 6 лет. У 27 (43,6%) пациенток основной группы рецидив диагностирован в течение 1-го года наблюдения, у 20 (32,3%) — в течение первых 3 лет, у 15 (24,2%) — спустя более 3 лет после лечения.
Оценка комплексной схемы лечения, проведенной у пациенток с рецидивирующей тяжелой дисплазией, показала, что при предоперационном применении комплексного отечественного препарата, содержащего интерферон альфа-2b, флуконазол, метронидазол и борную кислоту, в виде суппозиториев время подготовки к эксцизии составило у 87,5% пациенток менее 20 дней, в том числе у 40,3% менее 10 дней, у 46,8% — от 10 до 20 дней. Только у 8 (12,9%) женщин потребовалось более 20 дней для санации влагалища. Таким образом, в основном предэксцизионная подготовка была завершена в течение одного менструального цикла, что позволило осуществить LEEP или LLETZ в первую неделю после менструации; это является профилактикой кровотечений и постэксцизионного эндометриоза шейки матки.
Коррекция влагалищного микробиома на предоперационном этапе в сочетании с использованием радиоволновой методики эксцизии оказала благоприятное воздействие на последующую репарацию тканей шейки матки. Сроки эпителизации менее 4 нед отмечены у 21 (33,8%) пациентки, у 29 (46,8%) женщин заживление завершилось в сроки от 4 до 6 нед, полная эпителизация зоны эксцизии в сроке 6—8 нед отмечена у 12 (19,4%) женщин.
рН влагалища через 6 мес после лечения сохранялся ниже 4,5 у 31 (96,7%) обследованной 2-й основной группы. По данным теста ФЕМОФЛОР, умеренный и выраженный дисбиоз влагалища во 2-й основной группе диагностировался несколько реже, чем во 2-й контрольной группе (9,3% против 23,3% и 6,2% против 13,3% соответственно). Снижение количества лактофлоры и вагинальный кандидоз во 2-й контрольной группе диагностировались после завершения терапии несколько чаще по сравнению с этими показателями во 2-й основной группе (10,8% против 5,8% и 18,1% против 9,8% соответственно; р
>0,05).
После завершения курса терапии и реабилитации отмечено уменьшение числа курящих пациенток и имеющих избыточную массу тела по сравнению с исходными данными во 2-й основной группе: с 22 (69,4%) до 12 (38,7%) и с 11 (34,3%) до 8 (25%) соответственно. На наш взгляд, осознанное участие пациентки в лечебном процессе является важным компонентом терапии, помогает усилить мотивацию к лечению и повысить его эффективность.
У пациенток 2-й основной группы после лечения кольпоскопические картины, соответствующие норме, отмечены чаще, чем во 2-й контрольной (93,7% против 70%; р
≤0,05), аномальные типа HSIL — только в контрольной группе — 1 (3,3%) наблюдение, признаки воспаления несколько чаще встречались в контрольной группе — 20 (6,2%) (
р
>0,05). Нормальная цитограмма чаще регистрировалась в основной группе по сравнению с контрольной (81,3 и 53,3%;
р
≤0,05), койлоциты и клетки типа ASCUS несколько чаще отмечались в контрольной группе (16,7 против 6,3% и 13,3% против 3,1% соответственно).
Положительный тест на ВПЧ высокого канцерогенного риска после терапии отмечен у 6 (19,2%) пациенток 2-й основной группы (до лечения тест был положительным у 96,8%). У 50% из них реактивация вируса отмечена в течение первых 1,5 года наблюдения, других 50% — позднее.
Рецидив дисплазии после лечения диагностирован у 5 (15,6%) пациенток 2-й основной группы, в том числе CIN I — у 2 (6,2%), CIN II — у 1 (3,1%), CIN III — у 2 (6,2%). Рецидив CIN III в обоих наблюдениях отмечен при локализации в цервикальном канале. Прогрессирования процесса не было.
В контрольной группе рецидивирование отмечено в 6 (20%) наблюдениях. Рецидив CIN III выявлен у 3 (10%) пациенток, в том числе у 2 — при локализации CIN в цервикальном канале. Прогрессирование процесса отмечено у 1 (3,3%) пациентки. Всем проведена радикальная операция — гистерэктомия с придатками. CIN II выявлен у 2 (6,6%) пациенток спустя 1,5 года после лечения.
Положительная динамика состояния молочных желез клинически и по данным УЗИ после лечения констатирована у 20 (63,2%) пациенток 2-й основной группы.
Сочетанная гиперплазия эндометрия выявлена на этапе включения в исследование у 17,1% пациенток 2-й основной группы, после лечения при контрольной биопсии эндометрия патологии выявлено не было.
Были настроены на реализацию репродуктивной функции после терапии 13 пациенток. Беременность в течение 3 лет наступила у 9 (69,2%) из них и завершилась родами у 4 женщин, ранними самопроизвольными абортами у 3, у 2 беременность продолжается. В контрольной группе среди 12 женщин, настроенных на деторождение, беременность наступила у 6, при этом в течение первого года после лечения у 2 пациенток. Обе эти пациентки прибегли к медицинскому аборту в ранних сроках. У 1 пациентки беременность завершилась своевременными оперативными родами, у 1 — преждевременными родами в сроке 25 нед, у 2 произошел самопроизвольный выкидыш в сроке до 12 нед.
Таким образом, проведение у больных с рецидивирующей дисплазией шейки матки этапной комплексной терапии, включающей коррекцию образа жизни, пред- и постэксцизионную нормализацию микробиома влагалища, стимуляцию репарации и противовирусного иммунитета, назначение гормональной и дополнительной терапии, позволило повысить эффективность лечения, предупредить прогрессирование CIN, сохранить репродуктивную функцию пациенток.
Методика
Конизация слизистого слоя шейки матки может выполняться разными способами:
- ножевая предполагает хирургическое вырезание патологических участков;
- лазерная проводится при помощи лазерного луча и является более щадящей;
- электроконизация предполагает использование радиоволнового прибора.
Способ обработки шейки матки выбирается в соответствии с индивидуальными характеристиками пациентки. Немаловажное значение играет реализованность детородной функции.
При желании пациентки в будущем иметь детей, предпочтение отдается самому щадящему методу. По объему оперативного вмешательства можно выделить экономную конизацию, при которой удаленный участок составляет не более полутора сантиметров, и высокую – цервикальный канал иссекается на 2/3.
Ножевая
Около 40 лет назад эта методика была единственной. Удаление патологических участков осуществлялось обычным скальпелем. Процедура достаточно болезненная, несмотря на отсутствие нервных окончаний на слизистой шейки, поэтому проводится под общим наркозом.
В настоящее время ножевой метод остается предпочтительным для пациенток с подтвержденным раком. Главным плюсом такой процедуры является то, что она позволяет получить более полный материал для гистологического исследования, чем современные методы конизации.
К недостаткам ножевого лечения относятся: высокий риск осложнений, вероятность кровотечения, возможность инфицирования, формирование больших рубцующихся поверхностей и потеря функциональности шейки матки.
Лазерная
Данная методика считается боле предпочтительной, чем кардинальный способ лечения. Лазерная конизация осуществляется путем обработки шейки матки специальным лучом. Операция проводится без кровотечений и является практически безболезненной. Однако не во всех медицинских учреждениях можно ее сделать.
Данные статистики: исход патологии
Прогноз для пациентки зависит от стадии обнаружения патологии, а также от своевременности проводимого лечения. При поражении легкой степени вероятность самостоятельного восстановления слизистых оболочек довольно высока и составляет порядка 50%. Риск развития рака шейки матки не превышает 1%, потому поддаваться панике не стоит.
При раннем выявлении поражения принимается выжидательная тактика. Медики контролируют состояние женщины. Показано проведение кольпоскопии с периодичностью 1-2 раза за 6 месяцев. При обнаружении прогресса проводят удаление очага поражения.
При обнаружении умеренной дисплазии откладывать лечение бессмысленно, потому что есть риск перехода заболевания в 3 (запущенную) стадию. Тяжелая дисплазия при отсутствии терапии непременно трансформируется в рак и требует лечения по другому протоколу.
Стоит обратить внимание на следующие статистические данные:
- скрытое течение прослеживается у 10% пациенток, потому нельзя отказываться от регулярных гинекологических осмотров;
- на 1000 пациенток в возрасте от 25 до 35 лет приходится 1.5 случая выявления дисплазии ШМ;
- рецидив болезни при ее лечении на 2-3 стадии составляет 10%;
- при своевременном выявлении полное выздоровление наблюдается в 98% случаев;
- в 50% нелеченая дисплазия трансформируется в рак и оканчивается летальным исходом.
Внимание! Главной опасностью дисплазии ШМ является плоскоклеточный рак. Он прогрессирует стремительно и отличается бессимптомным течением. Именно поэтому гинекологи не рекомендуют игнорировать столь серьезную патологию.
Почему болезнь настолько распространена в России – сказать сложно. Скорее всего, причина заключается в халатном отношении женщин детородного возраста к собственному здоровью. Слабовыраженные симптомы часто игнорируются, а необходимость посещения врача рассматривается лишь после перехода патологии на позднюю стадию.
Реабилитация
В результате проведения электроконизации шейки матки при дисплазии послеоперационный период будет самым коротким и составит не более месяца. При кардинальном ножевом методе время заживления слизистой может увеличиваться в 3-6 раз.
Сразу после операции пациентка остается под наблюдением медиков не менее двух часов. При отсутствии осложнений ее выписывают для дальнейшего амбулаторного лечения. Важно выполнять рекомендации в течение всего восстановительного периода:
- исключить интимные отношения;
- не принимать ванну и не купаться в общественных водоемах;
- исключить тепловые процедуры, не загорать и не посещать баню;
- отказаться от использования тампонов, вагинальных средств;
- спринцеваться и использовать вагинальные свечи только по назначению врача;
- минимизировать физические нагрузки, не поднимать более 3 кг.
Через 2 недели после проведенного лечения рекомендуется показаться гинекологу для оценки качества результата выполненной манипуляции. В течение всего восстановительного периода у женщины могут отмечаться обильные выделения из влагалища. В первые недели они будут сукровичными, а позже станут прозрачными. Важно, чтобы они не имели гнойных примесей и неприятного запаха. К 10 дню после операции на обработанной зоне формируется струп.
Осложнения
Главным осложнением оперативного лечения считается рецидив дисплазии после конизации. В таком случае решается вопрос о необходимости удаления шейки матки целиком. Чтобы своевременно обнаружить развивающуюся повторно патологию, необходимо регулярно посещать гинеколога для профилактического осмотра. Обратиться к врачу незамедлительно после конизации надо при следующих симптомах:
- обильное кровотечение;
- отсутствие очередной менструации (как правило, конизация не влияет на цикл);
- повышение температуры тела;
- гнойные выделения из влагалища, неприятный запах;
- боли в животе, которые длятся более недели или усиливаются.
В результате проведенной операции может произойти инфицирование шейки и матки. При возникновении данного осложнения назначается лечение, предусматривающее использование антибиотиков местного и системного действия.
Беременность
Отзывы врачей свидетельствуют о том, что электроконизация шейки матки при дисплазии является самым лучшим вариантом лечения, если в дальнейшем планируется беременность. Операция не препятствует зачатию, однако снижает шансы его скорого наступления. Дело в том, что после конизации цервикальный канал частично теряет способность вырабатывать слизь, которая необходима для транспортировки сперматозоидов.
Отзывы женщин рассказывают, что проблемы могут начаться при вынашивании ребенка. Из-за частичного удаления шейки на протяжении всей беременности сохраняется угроза преждевременных родов. Если во время гестации возник рецидив дисплазии 3 степени, то лечение осуществляется после родов. При этом родоразрешение проводится посредством кесарева сечения.
Лечение дисплазии: современные методики
Прижигание представляет собой основной метод современной медицины, предназначенный для лечения эрозии. Действие обеспечивается за счет воздействия жидкого азота, лазера или электрокоагуляции. В тяжелых случаях используют методику электроконизации. Обязательным условием, обеспечивающим выздоровление, является отказ от случайных половых связей, избавление от болезней, передающихся половым путем, отказ от никотиновой зависимости.
Наибольший риск перерождения дисплазии в рак у пациенток, инфицированных онкогенными штаммами вируса папилломы человека. В этом случае необходимо обеспечить должное противовирусное воздействие и остановить внимание пациентки на необходимости приема иммунных препаратов.
Обнаружение дисплазии всегда представляет собой показание для проведения прижигания, несмотря на то, что поражение первой степени успешно лечится при помощи различных медикаментозных препаратов. Доказано, что эффективность радикальных методов несколько выше и это позволяет снизить риск развития злокачественного процесса у пациентки.
Существует ограниченный перечень противопоказаний к проведению прижигания:
- выраженные деформации шейки матки;
- грубые рубцы на поверхности слизистых оболочек;
- подозрение на развитие доброкачественного или злокачественного опухолевого процесса с локализацией в яичниках или матке;
- период менструального кровотечения;
- беременность и грудное вскармливание.
Временным противопоказанием к проведению операции является наличие инфекционных или воспалительных процессов с локализацией в органах репродуктивной системы. В таком случае прижигание проводят сразу после устранения заболеваний.
Внимание! При дисплазии 3 степени методика криодеструкции не применяется, потому что не проявляет собственную эффективность.
Электрокоагуляция дисплазии шейки матки
Подобная методика проста, но имеет как преимущества, так и недостатки. Из-за проявления побочных реакций в раннем послеоперационном периоде и болезненности процесса заживления ее считают устаревшей. Принцип действия заключается в том, что ток высокой частоты проходит через поврежденные участки шейки матки, пораженные дисплазией. Под таким воздействием обеспечивается частичное омертвение пораженных клеток. Методика электрокоагуляции обеспечивает разрушение массивных фрагментов тканей, потому процесс восстановления затягивается.
Основным преимуществом подобной методики является ее доступность и невысокая стоимость услуги. Оборудование, необходимое для проведения прижигания есть в каждой муниципальной клинике, потому лечение проходит по полису медицинского страхования. Процесс занимает не более 30 минут.
Современные медицинские центры постепенно отказываются от использования этого метода терапии, потому что он имеет массу отрицательных сторон. Например, процесс восстановления отличается сложностью и продолжительностью, присутствует риск развития осложнений вследствие инфицирования.
Лазерное прижигание дисплазии шейки матки
Лазерное прижигание имеет массу преимуществ в сравнении с другими методами лечения дисплазии, потому активно используется в лечении разнообразных гинекологических патологий. При помощи действия оборудования врач точно, но прицельно действует на пораженные ткани, провоцируя их испарение. Существенным недостатком этого популярного метода является то, что возможность забора образцов для гистологического исследования – отсутствует.
Перечень основных преимуществ метода:
- направленное действие;
- контролируемая глубина влияния;
- отсутствие деформации шейки матки;
- отсутствие грубых рубцов;
- продолжительность периода восстановления около 5 недель;
- время проведения вмешательства 7-10 минут.
Подобная манипуляция требует использования специального и дорогостоящего медицинского оборудования, которое доступно не всем центрам.
Радиоволновое прижигание дисплазии шейки матки
Прижигание эрозии обеспечивается при помощи специального электрода. Он воздействует на ткани шейки матки при помощи радиоволн высокой частоты. Технология рассматривается как новая, но в то же время проверенная. Радиоволновая хирургия активно используется в гинекологии и уже доказала собственную эффективность.
За счет прицельной точности в ходе операции врач может уничтожить даже мелкие очаги при этом, не повредив здоровые ткани. Медицинские манипуляции могут быть реализованы даже в амбулаторных условиях. Риск инфицирования поверхностей сводится к минимуму, потому что контакт радионожа и пораженной поверхности отсутствует. После заживления в зоне обработки рубец не формируется, а общее время процедуры составляет около 10 минут.
Внимание! В первые несколько суток после вмешательства у пациентки появляются сукровичные выделения, повышается температура тела. Такие побочные реакции являются нормой и не требуют дополнительного вмешательства.
Криодеструкция дисплазии шейки матки
На участок с предполагаемой дисплазией воздействуют жидким азотом при помощи специального устройства. Средство обеспечивает промерзание клеток на глубину 4-5 мм, потому для достижения лечебного результата требуется несколько процедур. По этому методу часто лечат умеренную дисплазию.
За счет воздействия холодом обеспечивается выраженное обезболивание пораженной зоны. В области воздействия образуется мягкий и незаметный рубец, женщина не испытывает трудностей с возбуждением при половых контактах. Вероятность влагалищного кровотечения сводится к минимуму, как и риск других осложнений.
Послеоперационный период занимает около 3 недель. В это время происходит отторжение пораженных тканей из влагалища. Вероятно появление гнойных выделений, обильность которых зависит от объемов зоны обработки.
Все что должен знать пациент об электронизации шейки матки
Электроконизация шейки матки – что это такое? При подозрении развития злокачественного новообразования, проводится гистологическое исследование. Для получения биологического материала и лечения патологии, врачи назначают – электроконизацию, основанной на иссечении части органа, посредством применения тока. По окончании операции, полученный материал передается лаборантам для гистологического исследования.
Электроконизация шейки матки
Что такое электроконизация
Электроконизация шейки матки – иссечение конусовидного участка репродуктивного органа женщины, посредством применения электрического тока. При хирургическом вмешательстве, удаляется: шейка, канал матки. Во время операции используются петлевидные электроды различных размеров. Несмотря на удобство использования этого метода, он имеет недостаток – при применении электродов, специалист не может контролировать глубину иссечения органа. Присутствует риск развития: кровотечения, рецидива раковой опухоли, сужение шейки матки.
Показания
Электродиатермоконизация шейки матки назначается при обнаружении: патогенных изменений, дисплазии эпителия. Основными показаниями являются:
- выявление зон изменения эпителия шейки матки;
- обнаружение патогенных клеток;
- дисплазия органа 2–3 степени – больная не ощущает симптомов заболевания, но при отсутствии лечения, могут развиться осложнения;
- эрозивные изменения шейки;
- ороговение слизистой органа (лейкоплакия);
- рубцовые изменения шейки – развивается из-за получения разрывов во время, травм;
- образование полипов;
- повторная дисплазия после оперативного вмешательства (электродиатермоконизация шейки матки, криодекструкции, лазерной вапоризации);
- эктропион – выворот слизистой органа.
Главным причинами проведения электроконизации считается: получение биологического материала для гистологического исследования, лечение злокачественных новообразований.
Противопоказания
Если имеется воспалительный процесс, проведение электроконизации запрещено. К главным противопоказаниям относятся:
- инвазивная форма онкологического заболевания;
- острая форме инфекционных патологий, воспалительные процессы;
- невозможно определение границы пораженных тканей;
- зона поражения раковыми клетками обширнее, нежели технические возможности оперативного вмешательства;
- плохая свертываемость крови;
- хронические патологии (сахарный диабет, сердечная недостаточность, гипертония, заболевания печени, почечная недостаточность).
Цель проведения
Главная цель проведения оперативного вмешательства – удаление патологических тканей, пораженных раковыми клетками. Электродиатермоконизация шейки матки позволяет решить две основные проблемы: выявление и лечение раковой опухоли.
- Происходит удаление тканей, пораженной раковыми клетками. Это позволяет добиваться положительной динамики в лечении раковой опухоли.
- На основе полученных материалов, лаборант проводит гистологическое исследование тканей.
- При не инвазивной форме рака, иссечения конусовидного участка органа достаточно чтобы полностью излечится от рака.
Как проводится оперативное вмешательство
Электроконизация – современный метод диагностики и лечения не инвазивной формы рака, при котором больной необязательно ложиться в стационар, все манипуляции проводятся амбулаторно. Непосредственно перед назначением даты операции, женщине предстоит сдать ряд анализов, по которым определяется возможность проведения операции.
Подготовка к электроконизации
Оперативное вмешательство проводится после завершения менструального цикла, на 1–2 сутки. Это объясняется тем, что в этот период, в женском организме имеет большое количество эстрогена, способствующего скорейшему выздоровлению больной.
Прежде чем записаться на операцию, женщине необходимо подготовиться. За месяц до запланированного хирургического вмешательства, пациентке необходимо пройти: консультацию узких специалистов, некоторые обследования:
- консультация гинеколога, иммунолога;
- мазок на определение микрофлоры влагалища;
- УЗИ органов малого таза, лимфатических узлов;
- биопсию.
При выявлении патологий, время проведения хирургического вмешательства переносится до полного купирования воспалительного процесса. За две недели до операции, женщине предстоит пройти несколько обследование, сдать анализы.
- ОАК, ОАМ.
- Кровь на сифилис, антитела к ВИЧ и вирусным формам гепатита.
- Гемостазиограмма.
- Осмотр, консультация гинеколога.
- Кровь на группу крови, резус-фактор.
- Флюорография за последний год.
- ЭКГ.
- Консультация терапевта.
Особенности проведения хирургических манипуляций
При проведении электроконизации используется оборудование для электроволновой хирургии «Сургитрон». Это электрогенератор в комплекте с которым, имеется набор электродов различного размера. Иссечение необходимого участка тканей проводится посредством воздействия высокочастотного тока.
Пораженные ткани удаляются петлевым электродом, размер которого заранее подбирает специалист. При проведении хирургического вмешательства, важно учитывать, что размер удаляемого участка тканей, должен на 3–4 мм превышать объемы пораженной зоны. Непосредственно во время операции, на электрод подается высокочастотный ток. Специалист начинает вращать электрод по кругу, вырезая ткани на глубину 5–8 мм.
Этот вид оперативного является самым распространенным и имеет ряд преимуществ:
- все манипуляции проводятся под местной анестезией;
- для проведения операции женщине необязательно ложиться в стационар;
- риск появления кровотечения минимизирован, благодаря быстрой коагуляции кровеносных сосудов;
- температура в зоне иссечения не превышает 55 °C, в связи с этим риск получения ожога равен нулю;
- весь полученный материал почти не имеет повреждений и лаборант может поставить диагноз с максимальной точностью;
- риск развития осложнений минимален.
Методы и особенности проведения операции
Проводится конизация шейки матки в условиях стационара, степень хирургического вмешательства и метод его проведения зависит от состояния пациентки и уровня патологических изменений. Назначается данная процедура при дисплазии различной стадии, эрозийных поражениях слизистой поверхности и при подозрении на раковую опухоль.
В процессе обследования лабораторными методами устанавливается наличие либо отсутствие раковых клеток. При положительном результате биопсии назначаются более углубленные исследования и соответствующее лечение.
Если диагностирован рак шейки матки последней стадии, то удаляется весь орган, чтобы предотвратить дальнейшее распространение метастаз и перерастание их в злокачественные новообразования на соседних участках.
В случае обнаружения дисплазии – преобладания атипичных клеток в эпитеальном слое, удаление поврежденного участка является необходимостью, при этом орган сохраняется. Чтобы предотвратить дальнейшее прогрессирование патологии, во время иссечения захватывается часть здоровой плоти (примерно пять миллиметров), что увеличивает размеры раневой поверхности, зато исключает риски рецидивных проявлений заболевания.
- Ножевой – конизация проводится с применением скальпеля. Метод считается самым травмирующим, поэтому применяется очень редко. Процедура довольно болезненная, что требует принятия мер по обезболиванию. Период заживления после иссечения тканей этим методом довольно длительный, часто возникают серьезные осложнения в виде кровотечений и инфицирования раны болезнетворными микроорганизмами. По мере заживления образуется рубец, который может стать проблемой при наступлении беременности и последующих родах.
- Лазерный – новейший метод проведения гинекологических операций. С помощью лазера достигается максимальная точность удаления измененных слоев эпителия. В ходе операции специалист имеет возможность менять глубину воздействия и размер удаляемого участка. Цервикальный канал иссекается более аккуратно, что снижает риск возникновения послеоперационных осложнений. В период восстановления у пациентки могут наблюдаться незначительные кровянистые выделения, болевые ощущения тянущего характера, которые сохраняются непродолжительное время и чувство дискомфорта. После конизации шейки матки функциональность органа сохраняется, возможность вынашивания плода повышается в несколько раз. Метод достаточно дорогой, что является его существенным недостатком, так как для многих женщин остается недоступным.
- Петлевой – проводится специальной электродной петлей, через которую проходит переменный ток. Назначается для удаления кист, полипов, а также применяется при конизации, если есть подозрения на наличие атипичных клеток. Способ высокотехнологичный, позволяющий свести к минимуму болевые проявления и кровотечения после процедуры. Биологический материал, взятый при помощи электрической петли, практически не повреждается, что облегчает его дальнейшее исследование.
- Радиоволновой – самый распространенный и наименее травмирующий метод. Происходит коагуляция поврежденных тканей посредством воздействия на них высокочастотных волн, при этом отсутствует болезненность, так как мягкие ткани теряют чувствительность за счет отмирания нервных окончаний. После проведения конизации шейки матки радиоволновым методом полностью сохраняется детородная функция, а после процедуры опасность осложнений практически отсутствует.
Процедура проводится сразу после окончания месячных на 1-2 день (чтобы не было никаких выделений). При этом пациентке нужно заблаговременно подготовиться.
Минимум за месяц до планируемой даты конизации женщина должна пройти гинеколога, кольпоскопию, сдать мазки на микрофлору. Затем врач может назначить дополнительные исследования, такие как УЗИ органов малого таза, лимфатических узлов и пр.
За 14 дней до дня оперативного вмешательства пациентка должна сдать кровь на общий анализ, а также провериться на отсутствие ВИЧ, сифилиса, гепатитов В и С. Кроме того необходимы такие исследования:
- анализ мочи;
- ПЦР-исследование;
- посев из влагалища на наличие микрофлоры;
- гемостазиограмма;
- анализ крови на группу и резус-фактор.
Показанием к проведению конизации являются такие состояния у женщин:
- внутренние разрывы, рубцы и повреждения цервикального канала и шейки матки, образовавшиеся вследствие тяжелой родовой деятельности;
- подозрения на онкологию для диагностики или лечения;
- эктропион;
- дисплазия;
- полипы;
- эрозия и псевдоэрозия;
- гипертрофия и пр.
Именно ранняя диагностика дисплазии и конизация позволяют избежать превращения недуга в рак.
Рекомендации по профилактике осложнений
После хирургического удаления, остается открытая рана. Чтобы избежать осложнений женщине нужно снизить любое давление на ослабленный орган:
- воздержаться от половой близости в течение месяца;
- исключить применение тампонов во время менструаций, лучше отдать предпочтение гинекологическим прокладкам;
- избегать стрессовых ситуаций, морального перенапряжения;
- не принимать ванну (особенно горячую), лучше ограничиться прохладным душем;
- не поднимать тяжести весом более 3 кг;
- нормализовать режим дня, спать не менее 8 часов в сутки;
- принимать витаминные комплексы, повышающие функциональность иммунной системы;
- соблюдать правила интимной гигиены;
- использовать средства для интимной гигиены без ароматизаторов;
- правильно питаться, включить в меню блюда, богатые витаминами (фрукты, овощи, злаковые);
- избегать переохлаждения, перегревания;
- исключить прием препаратов, снижающих свертываемости крови.
Современные методы диагностики и лечения раковых опухолей, позволяют добиться максимально эффективного результата. Благодаря минимальному повреждению тканей при электроконизации, риск развития осложнений минимален.
Электроконизация шейки матки при дисплазии
Дисплазия шейки матки представляет собой предраковую патологию, которая характеризуется ростом атипичных клеток в эпителии. Дисплазия относится к одному из самых часто диагностируемых заболеваний у женщин репродуктивного возраста. По-другому патология называется преинвазивной онкологией или раком ин ситу.
Шейка матки является частью репродуктивной системы, которая соединяет маточное тело и влагалище цервикальным каналом. Шеечный канал препятствует попаданию инфекции из влагалища в матку, которая является стерильной. Это достигается благодаря анатомической узости канала и наличия специальных желез, продуцирующих защитную слизь. Поверхность канала выстлана цилиндрическими однослойными клетками.
Значительная часть шейки матки недоступна для осмотра. При гинекологическом обследовании можно визуализировать лишь её влагалищную часть, которую покрывают плоские многослойные клеточные элементы.
Эпителий шейки матки состоит из нескольких слоёв:
- базального;
- промежуточного;
- поверхностного.
Самый глубокий слой, называемый базальным, содержит незрелые округлые клетки с большим ядром. По мере их созревания, они поднимаются, подвергаясь уплощению. При дисплазии этот естественный процесс нарушается. Клетки приобретают признаки атипии.
При дисплазии возникают структурные изменения в шеечном эпителии. Нормальное деление на слои также утрачивается.
В развитии дисплазии выделяют 3 степени.
- В патологический процесс вовлекается не более трети толщины эпителия.
- Поражение более трети шеечного эпителия.
- Распространение атипичных клеток более чем на половину толщины эпителия.
Дисплазия 3 степени считается преинвазивным раком и отличается от онкологии отсутствием прорастания злокачественных клеток в строму. При 3 степени врачи прибегают к хирургическому лечению, например, конизации шейки матки.
Как эрозия перерождается в дисплазию
Точно определить, сколько времени потребуется для перехода эрозии в дисплазию сложно. Многое зависит от локализации поражения и его глубины. В большинстве случаях прогресс не стремительный и занимает около полугода.
Причины возникновения поражения могут быть следующими:
- активность онкогенных штаммов вируса папилломы человека типа 16 и 18;
- снижение иммунитета;
- неправильное питание, а именно недостаток свежих овощей и фруктов в рационе;
- наследственная предрасположенность;
- избыточный вес или ожирение 2-3 степени;
- длительный прием антибиотиков и комбинированных пероральных контрацептивов;
- хроническая усталость.
Могут ли проявляться боли при дисплазии шейки матки? Как правило, болевой синдром отсутствует, потому что шейка лишена нервных окончаний. Именно в этом и заключается опасность ее патологий – выявить болезнь на ранних стадиях самостоятельно практически невозможно.
Воздействия перечисленных факторов достаточно, чтобы спровоцировать переход эрозии шейки матки в дисплазию. В качестве основных причин, повышающих риск развития патологии у женщин репродуктивного возраста, выделяют: никотиновую зависимость, заражение ВПЧ, нехватка витаминов в организме.
Существуют 3 стадии развития патологии:
| Стадия | Описание |
| 1 стадия (легкая) | Характеризуется поражением 1/3 от всей глубины слизистых. |
| 2 стадия (умеренная) | Захватывает 2/3 от глубины. |
| 3 стадия (тяжелая) | Выявляют поражение всех слизистых оболочек влагалища, но не затрагивается базальная мембрана. |
Медики рассматривают еще четвертую, последнюю стадию, но она не входит в современную классификацию болезни. На этом этапе диагностируют так называемый предрак.
Причины возникновения
В современной гинекологии доказана прямая связь между появлением дисплазии, в частности, 3 степени и ВПЧ. Этот вирус, поникая в клетку, вызывает клеточные мутации. Однако, зачастую для развития патологического процесса необходимо воздействие некоторых негативных факторов:
- отягощённый семейный анамнез;
- хронические воспалительные и инфекционные процессы в малом тазу;
- нарушения в иммунной системе;
- курение;
- гормональный дисбаланс;
- начало половой жизни в юном возрасте;
- травмы шейки матки;
- беспорядочная интимная жизнь.
Клиническая картина при дисплазии в большинстве случаев отсутствует. Характерные признаки обычно появляются при прогрессировании заболевания в 3 степени и после присоединении инфекции.
Среди симптомов при развитии дисплазии 3 степени можно выделить:
- тянущие тазовые боли;
- дискомфорт половых органов;
- патологические выделения, которые могут сопровождаться неприятным запахом;
- контактные выделения во время полового акта и гинекологического осмотра.
Как обнаружить дисплазию
Начальным этапом диагностики по гинекологическому профилю является осмотр шейки матки женщины в зеркалах. Уже на этом этапе могут быть обнаружены нарушения, указывающие на развитие патологического процесса. К перечню важных диагностических критериев относят:
- изменение оттенка стенок влагалища;
- гипертрофия слизистых оболочек;
- блеск в области зева;
- нехарактерная равномерность эпителия;
- наличие белесых очагов на слизистой.
При выявлении подобных изменений используют другие методы, позволяющие подтвердить предположительный диагноз:
- ПАП-тест. В ходе обследования проводится цитологическое изучение эпителиальной ткани под микроскопом. Забор образцов тканей для обследования проводят с разных областей шейки для получения точной диагностической картины. Такой метод позволяет получить точную и информативную картину, определяет маркеры, провоцирующие процесс. Позволяет выявить ВПЧ.
- Расширенная кольпоскопия. Используется как дополнительный метод диагностики в случае. Когда точности цитологического исследования недостаточно. Для подтверждения диагноза и обнаружения атипичных участков на шейку матки наносят специальные реагенты (раствор уксусной кислоты и Люголь).
- Биопсия. Для проведения обследования по этому методу требуется забор биологического материала. Метод позволяет определить не только степень, но и характер дисплазии, исключает развитие онкологии.
- ПЦР диагностика. Направленный иммунологический метод, позволяющий обнаружить ВПЧ. По его результатам медики могут подобрать наиболее удобный способ медикаментозного и хирургического лечения.
Внимание! Для определения точного диагноза необходим биохимический анализ крови, исследование баланса гормонов.
Основная цель врача, проводящего обследование – дифференцировать диагноз. Схожую клиническую картину и проявления имеют такие заболевания:
- лейкоплакия;
- цервицит и другие инфекционные патологии;
- эрозия и псевдоэрозия.
Особое внимание дифференциальной диагностики дисплазии необходимо уделить старшей возрастной группе. У пациенток в менопаузе появление видимых изменений слизистой шейки матки часто обусловлено естественным процессом. Проявляется на фоне выраженных колебаний гормонального фона (недостаток эстрогена).
Диагностика и лечение
Для выявления патологии применяются следующие методы:
- гинекологический осмотр;
- мазок на онкоцитологию;
- ПЦР-исследование;
- расширенная кольпоскопия;
- биопсия;
- анализ крови на онкомаркеры, сифилис и ВИЧ;
- бакпосев и общий мазок;
- гормональная диагностика;
- УЗИ органов малого таза.
Основным методом исследования является цитологическая диагностика, которая представляет собой забор материала из разных участков шейки матки для выявления атипичных клеток и воспалительного процесса.
Лечение дисплазии 3 степени преимущественно хирургическое, которое заключается чаще всего в конизации шейки матки. На начальном этапе или при беременности возможно применение наблюдательной тактики. Пациентка регулярно посещает врача и проходит обследование.
Прогрессирование патологии является показанием к использованию хирургических методик.
- Конизация. Это вмешательство относится к органосохраняющим тактикам. Операция предполагает удаление области шейки матки, включающей атипичные ткани, в форме конуса. Ампутированные ткани содержат фрагменты шейки матки и цервикального канала. Манипуляция осуществляется как с диагностической, так и лечебной целью.
Конизация шейки матки может проводиться разными способами.
1. Ножевая. Операция выполняется скальпелем. В современной гинекологии такая конизация применяется нечасто из-за высокой травматичности. Кроме того, существуют более эффективные и щадящие методики.
2. Лазерная. Конизация при помощи лазерного луча считается самой дорогостоящей.
3. Электроконизация. По-другому данное вмешательство называется петлевой конизацией. Это самая распространённая разновидность конизации.
- Высокая ампутация. При такой тактике происходит радикальная ампутация шейки матки, которая рекомендуется при дисплазии 3 степени и онкологической настороженности. Метод высокой ампутации позволяет остановить прогрессирование злокачественного процесса.
Перед конизацией и другим хирургическим вмешательством женщина выполняет необходимое обследование:
- общий и биохимический анализ крови;
- диагностику сифилиса и гепатитов;
- общий анализ мочи;
- мазок на флору;
- мазок методом ПЦР;
- кольпоскопию;
- биопсию.
Конизация шейки матки может иметь негативные последствия.
- При конизации изменяется анатомия шейки матки. В результате цервикальный канал остаётся расширенным, что может приводить к хроническим инфекциям.
- Существует риск рецидивов в случае технической сложности выполнения конизации, который вызван некоторыми анатомическими особенностями шейки матки.
- После выполненной конизации способность шейки трансформироваться в родовой канал утрачивается, что вызывает необходимость проведения хирургического родоразрешения.
- Конизация не влияет на репродуктивную способность женщины, однако, она увеличивает риски невынашивания и преждевременных родов.
- При конизации хирургу сложно рассчитать глубину воздействия, в результате могут захватываться слишком обширные участки здоровой ткани. Иногда у нерожавших пациенток врач ампутирует незначительный объём поражённого эпителия, что приводит к рецидиву дисплазии.
В целях профилактики развития воспалительного процесса, пациентке проводят антибактериальное лечение. При выраженном болевом синдроме показан приём обезболивающих средств.
В течение месяца после конизации женщине не рекомендовано посещать сауну или бассейн, поднимать тяжести и использовать тампоны. Половая жизнь также запрещена в связи с риском присоединения инфекции и излишней травматизации повреждённой шейки матки. Повторная кольпоскопия проводится не ранее, чем через четыре месяца после конизации шейки матки.
Материал и методы
На первом этапе с целью выявления факторов риска рецидива и прогрессирования CIN проведена ретроспективная оценка тактики ведения 122 пациенток с тяжелыми формами дисплазии шейки матки — цервикальной интраэпителиальной неоплазией II—III степени (CIN II—III) за период с 2007 по 2015 г. Из них 60 пациенток (1-я контрольная группа), у которых после лечения не было рецидивов заболевания, и 62 больные (1-я основная группа), у которых диагностирован рецидив дисплазии. На втором этапе на основании данных анализа факторов риска у пациенток с рецидивирующей дисплазией разработан этапный алгоритм тактики ведения CIN II—III, включающий расширение диагностического спектра обследования, коррекцию образа жизни, предэксцизионную подготовку с последующим проведением радиоволновой эксцизии, постэксцизионную стимуляцию репарации, стимуляцию противовирусного иммунитета, проведение реабилитации. Расширенный спектр обследования включал: цитологическое исследование, расширенную кольпоскопию, проведение теста ФЕМОФЛОР для оценки микробиома влагалища, определение рН влагалища, исследование для определения ВПЧ высокоонкогенных типов (14) с установлением количественной нагрузки, УЗИ органов малого таза и молочных желез (у женщин старше 40 лет — маммография), исследование гормонального статуса, биопсию эндометрия. Предэксцизионная подготовка проведена с применением комплексного отечественного препарата, содержащего интерферон альфа-2b, флуконазол, метронидазол и борную кислоту в виде суппозиториев вагинально на ночь в течение 10 дней, эксцизия типа LEEP/LLETZ (loop electrosurgical excision procedure — петлевая электроконизация шейки матки/large loop excision of transformation zone — широкая петлевая эксцизия зоны трансформации) проводилась на аппаратах ФОТЕК 140 или Сургитрон, постэксцизионная стимуляция репарации осуществлялась вагинальным гелем, содержащим дигидрокверцетин (0,4%), лецитин (3%), глицин (5%), антисептик растительного происхождения (0,01%), в течение 10 дней. Стимуляция противовирусного ответа после эксцизии патологического очага проводилась отечественным препаратом растительного происхождения, являющимся биологически активным полисахаридом, полученным из растения Solanum tuberosum
(паслен клубненосный) и относящимся к классу высокомолекулярных гексозных гликозидов сложного строения (панавир). Данный препарат оказывает непосредственное воздействие на вирус, а также дает дополнительный иммунокорригирующий эффект. Препарат назначался по схеме, состоящей из 5 внутривенных инъекций, проводимых с интервалами 48—72 ч. Реабилитация включала коррекцию гормональных нарушений и назначение дополнительной терапии биологически активной добавкой на 6 мес. У пациенток, планировавших беременность, после завершения курса реабилитации на 6 мес назначали препарат дидрогестерон по 20 мг/сут с 16-го по 25-й день менструального цикла; у женщин, не планировавших реализацию детородной функции, применялись комбинированные оральные контрацептивы или вагинальная система, содержащая этоногестрела 11,7 мг, этинилэстрадиола 2,7 мг; в пролонгированном режиме 42+7. Дополнительная терапия осуществлялась биологически активной добавкой — источником флавоноидов, содержащей 45 мг эпигаллокатехин-3-галлата и 90 мг индол-3-карбинола в дозе по 2 капсулы 2 раза в сутки в течение 6 мес. При наличии пролапса влагалища пациенткам был проведен 6-месячный курс тренировок для укрепления мышц тазового дна (ТМТД) с вагинальными конусами (5 пациенток) или миниинвазивная перинеопластика (3) в сочетании с курсом ТМТД.
На третьем этапе была сформирована 2-я основная группа пациенток (32 женщины, в том числе 13 планировавших беременность после завершения терапии), пролеченных, согласно разработанному алгоритму ведения. Эффективность лечения сопоставлена с общепринятой схемой ведения, включавшей эксцизионное воздействие со стимуляцией противовирусного иммунитета препаратом растительного происхождения, являющимся биологически активным полисахаридом, полученным из растения Solanum tuberosum
(2-я контрольная группа — 30 пациенток, в том числе 12 планировавших деторождение после лечения).